Histoire évolutive des phasmes et des phyllies
Par Benoît GILLES
L’Ordre des Phasmatodea (phasmes et phyllies), composé de plus de 3 100 espèces et 500 genres, constitue l’un des plus anciens groupes d’insectes. Ils sont populaires pour leur capacité à se camoufler dans la végétation. Leur morphologie, arborant parfois des formes extravagantes, les fait ressembler à des brindilles, à des feuilles ou encore à de l’écorce dans le but de les rendre invisibles aux yeux des prédateurs. Ce mimétisme peut être homochromique (couleur) ou homomorphique (forme), voire les deux en même temps.

La quasi-totalité des espèces de « phasmes », phytophage et nocturne, se rencontre principalement dans les régions tropicales et sub-tropicales.
La systématique des Phasmatodea reposant jusqu’à aujourd’hui essentiellement sur des critères morphologiques et géographiques, la classification des taxons s’avère peu représentative de leur histoire phylogénétique (relation de parenté entre les êtres vivants) et biogéographique. Bien que des études phylogénétiques aient été réalisées ces dernières années, les données, souvent restreintes, n’ont pas permis d’apporter des conclusions fiables sur leur évolution qui demeure de ce fait un mystère.
Une équipe internationale, menée par l’entomologiste allemand Sven Bradler (Département de l’Evolution animale et de la Biodiversité, Université de Göttingen, Allemagne) a entrepris d’éclaircir ce mystère en menant une étude basée sur 27 nouveaux transcriptomes (ARN issus de la transcription du génome) provenant d’un échantillonnage représentatif de la diversité du groupe à travers la planète (hormis l’Afrique).
A l’aide d’outils moléculaires et génétiques, les scientifiques ont pu estimer le temps de divergence entre les différentes espèces (phylogénie) et, ainsi, reconstituer l’histoire biogéographique du groupe (phylobiogéographie).
Les résultats de leur étude ont été publiés en octobre 2019.
Nouvelle classification des « phasmes »
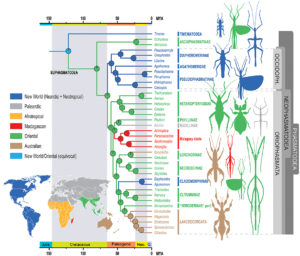
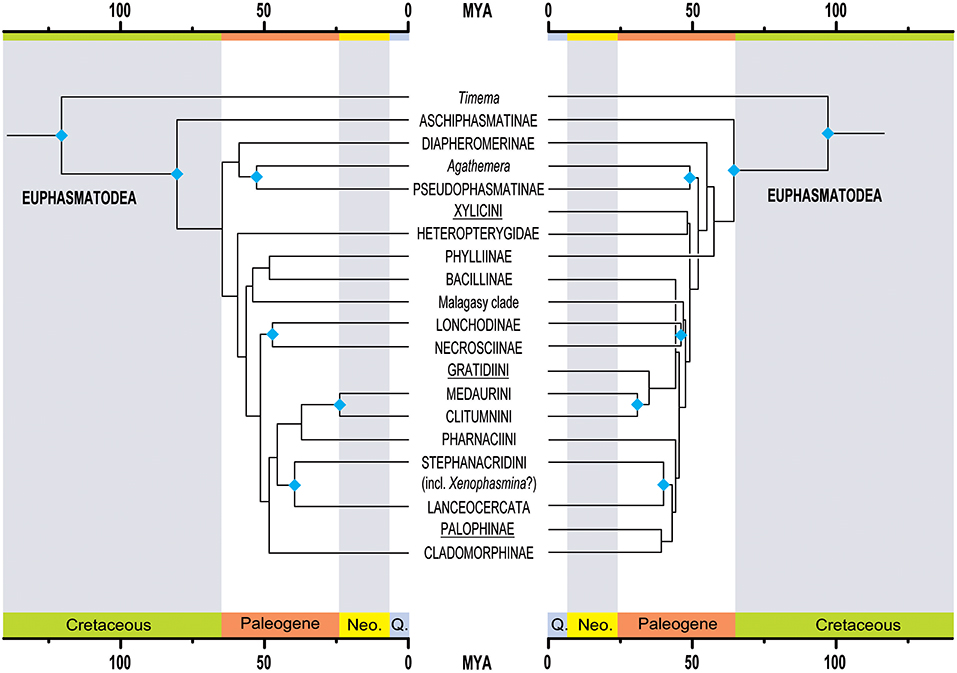
Les premiers éléments de l’étude confirment la place des Phasmatodea par rapport aux autres grands groupes établie par des analyses moléculaires antérieures. L’apparition des Phasmatodea survient après celle des Dermaptères (perce-oreilles), des Plécoptères (perles), des Dictyoptères (termites et mantes) et des Embioptères (figure 1 ci-dessous).
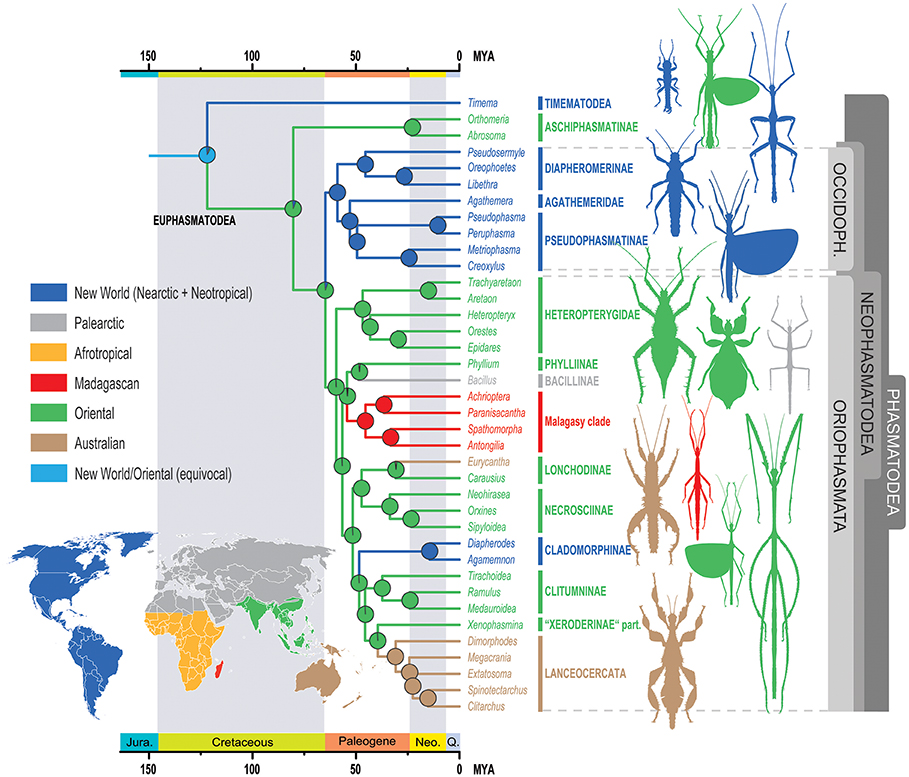
L’originalité des résultats publiés réside notamment dans la mise en évidence de liens entre géographie et proximité génétique (espèces apparentées) auparavant insoupçonnés. Les analyses génétiques regroupent les espèces en deux grandes zones géographiques : celles appartenant à l’Ancien-Monde et celles appartenant au Nouveau-Monde. Les auteurs proposent de nommer ces deux nouveaux clades (groupes) : Oriophasmata (« Phasmides d’Orient », Ancien-Monde) et Occidophasmata (« Phasmides occidentaux », Nouveau-Monde) (figure 1 ci-dessus et figure 2 ci-dessous).
Chose surprenante, aucun schéma taxonomique ou caractère morphologique n’avait jusqu’alors suggéré cette répartition.
– Occidophasmata
Le clade des Occidophasmata se subdivise en deux clades dominants également associés à la géographie : les Diapheromerinae se rencontrant en Amérique du Nord et les Pseudophasmatinae (=Pseudophasmatidae pour certains auteurs) se rencontrant quant à eux en Amérique du Sud (figure 2). La caractérisation de ces groupes repose essentiellement sur la présence ou l’absence d’un champ triangulaire au sommet du tibia.

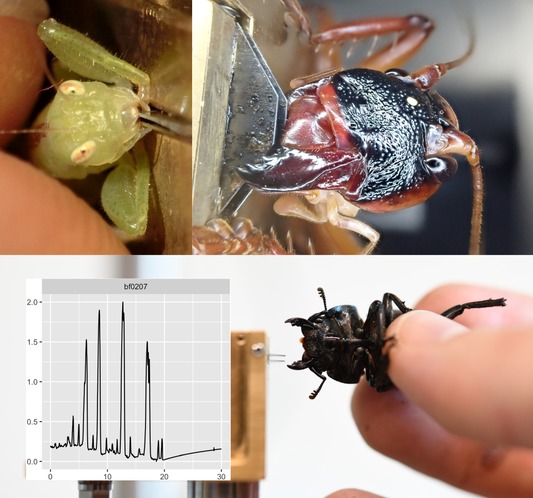
Au sein du groupe des Pseudophasmatinae, la position phylogénétique du genre Agathemera (Amérique du Sud) (photo 1 ci-contre), composé de huit espèces caractérisées par l’absence d’ailes et une forme corpulente, est restée longtemps une énigme.
A partir de critères morphologiques, le genre a été placé successivement et à plusieurs reprises au sein des groupe sœurs des Euphasmatodea ou des Pseudophasmatinae. Les résultats obtenus en 2019 corroborent partiellement le rattachement de ce genre au groupe des Pseudophasmatinae.
– Oriophasmata
Parmi les Oriophasmata, les changements qu’apporte l’étude concernent principalement le placement de la sous-famille des Phylliinae (véritables phasmes « feuilles » : Phyllium philippinicum – photo 2 ci-dessous) au sein des Euphasmatodea. Des études moléculaires antérieures proposaient une divergence récente de ces lignées. Là encore, les données biogéographiques soutiennent cette phylogénie. Bien que les Phylliinae aient actuellement une aire de répartition essentiellement asiatique, des fossiles âgés de -47 millions d’années témoignent de l’origine européenne des ces insectes.

Du côté de l’Afrique, un clade monophylétique (groupement d’espèce ayant un ancêtre commun vs polyphylétique) spécifique à Madagascar a également été identifié. Celui-ci est constitué des familles des Anisacanthidae (Paranisacantha) et des Phasmatidae (Spatomorpha), de la tribu des Achriopterini (Achrioptera) et de la sous-famille des Antongiliinae (Antongilia).
De son côté, le clade des Lonchodidae (Oriophasmata), comprenant les sous-familles Lonchodinae et Necrosciinae, s’est récemment fortement diversifié (radiation évolutive) en plus de 1 000 espèces, représentant ainsi près de 30% des Phasmatodea décrits.
Diversification des Phasmatodea
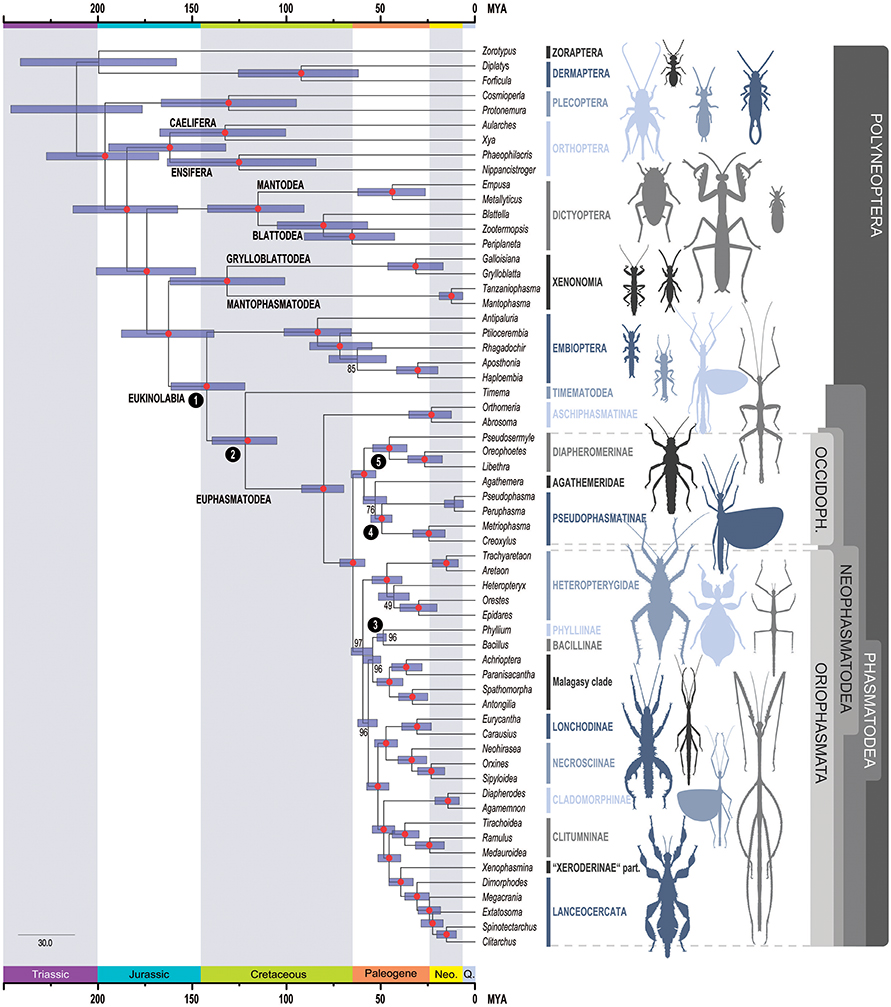
Les résultats de l’étude apportent de nouvelles estimations quant aux périodes de diversification des Phasmatodea (figure 3 ci-dessous).
Le premier évènement de radiation, qui concerne la scission du clade Euphasmatodea avec celui des Timematodea (représenté actuellement par le genre Timema) (figure 1), dont les premières estimations reposaient sur la découverte en Chine de fossiles datés du Mésozoïque entre -103 et -95Ma, trouverait une origine plus ancienne autour de -121Ma (Crétacé).
Un second évènement de radiation a eu lieu entre les espèces « bâtons » et les espèces « feuilles ». Estimée précédemment à -61Ma, la scission se serait déroulée autour de -80Ma.
La divergence des deux grands clades géographiques, les Orio- et les Occidophasmata, aurait quant à elle débuté autour de -64Ma (Crétacé), puis la divergence des Occidophasmata d’Amérique du Nord et ceux d’Amérique du Sud autour de -58,9Ma (Paléogène).
Chez les Oriophasmata, les évènements de radiations se seraient déroulés à la même période (-59,5Ma), lorsque les Heteropterygidae vivant au sol auraient divergé du reste du clade. La diversification des Heteropterygidae a quant à elle débuté au début du Paléogène autour de -46,4Ma.
La scission entre les clades des Phyllinae et des Bacillinae aurait débuté avant la séparation de Madagascar avec le continent africain, soit autour de -56,6Ma. Un événement de radiation du clade malgache aurait quant à lui débuté plus récemment entre -38,2 et -52,1 Ma.
La présence aujourd’hui de phasmes « bâtons » sur l’île corrobore l’hypothèse d’une colonisation par ces insectes après sa séparation avec l’Afrique (-38 et -51Ma).
Les résultats de cette étude permettent également d’estimer d’autres événements de radiation majeurs chez les Oriophasmata, entre les Lonchodinae, les Necrosciinae (-47,3Ma) et les Clituminae (-37,3Ma) par exemple.
Dans la région Indo-Australienne, le clade des Cladomorphinae néotropicaux auraient divergés de ceux de l’actuelle Australie avant la séparation de l’Antarctique australien et sud-américain, soit entre -42,6Ma et -54,6Ma.
En résumé, cette étude, reposant sur la technique de l’horloge moléculaire, corrobore une diversification récente des Phasmatodea s’étant principalement déroulée durant le Crétacé (autour de -66Ma).
La cause de cet évènement récent et du succès des Euphasmatodea n’est pas encore bien comprise. Une des explications réside dans un phénomène de co-évolution entre ces insectes et les Angiospermes. Des associations écologiques similaires comme les relations proies/prédateurs et le mimétisme ont cependant été découvertes dans des fossiles d’espèces de phasmes « bâtons » datés du Crétacé et vivant dans des forêts de Gymnospermes.
Une autre explication repose sur le développement d’innovations majeures comme le transfert horizontal de gènes de pectinases de bactéries intestinales dans le génome de certaines espèces, améliorant leur capacité à dégrader des Angiospermes, ou le développement d’œufs en forme de graine à coque dure. Il est également possible que la diversification de ces insectes soit le fruit d’une combinaison de facteurs multiples.
Le saviez-vousLes juvéniles de l’espèce Extatosoma tiaratum ont la particularité, durant le premier stade larvaire, de mimer dans la morphologie et le comportement une espèce de fourmi (Leptomyrmex erythrocephalus) : déplacements rapides, pattes antérieures relevées à la manière des antennes de la fourmi. Les œufs, comme chez de nombreuses autres espèces, présentent au niveau du capitulum (capsule de sortie) une « boule » composée d’éléments nutritifs (voir photos ci-dessous). Ainsi, une fois pondu et tombé sur le sol, l’œuf est récolté par une fourmi puis ramené au nid où il sera stocké et mis à l’abris des prédateurs le temps de leur développement. Les juvéniles, après l’éclosion, sortent de la fourmilière sans être inquiétés par les fourmis en raison de leur mimétisme morphologique, mais aussi par la présence de phéromones spécifiques sur leur cuticule inhibant toute agressivité de la part des fourmis.  |
Histoire biogéographique
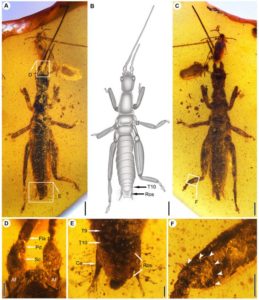
L’étude conforte l’origine orientale des Phasmatodea : la découverte récente en Birmanie de fossiles d’individus datant du Crétacé et proches du clade des Timematodea appuie cette hypothèse (figure 4). Cependant, bien que la région ancestrale des Aschiphasmatinae et des Neophasmatodea soit considérée comme orientale, des analyses complémentaires doivent toutefois être entreprises afin de valider cette hypothèse.
Compte tenu d’une diversification récente, la reconstruction de l’arbre phylogénétique et de la biogéographie des phasmes semble plutôt simple. Les différents évènements de radiations peuvent s’expliquer par la géographie et des événements de dispersion.
La colonisation de Madagascar par des phasmes « bâtons » après sa séparation du continent africain et celle de l’Europe méridionale par une lignée de phasmes « feuilles » (Phylliinae) en sont des exemples (figure 2 ci-dessus).
Plus étonnant encore, le clade des Cladomorphinae d’Amérique Centrale et du Sud serait originaire d’Asie du Sud-Est. La colonisation du contient américain résulterait d’une dispersion transocéanique, probablement transpacifique, ou via l’Antarctique lorsque celui-ci était encore relié à l’Australie et à l’Amérique du Sud. Des cas de dispersions sur de telles distances vers l’est et à travers le Pacifique ont déjà été signalés chez des arthropodes : les araignées côtières Amaurobioides (Araneae) et les pyralles métallifères (Lepidoptera – Choreutidae) par exemple.
La dispersion transocéanique a joué un rôle important à plusieurs reprises dans l’évolution des Phasmatodea, notamment dans l’Océan Indien avec l’Australie et l’archipel des Mascaraignes (lien Ornebius) (figure 4 ci-dessous).
|
Comment des phasmes peuvent-ils traverser les océans sur de telle distance ? Plusieurs hypothèses sont proposées comme le transport d’individus sur des îlots de végétations, des œufs flottant à la surface de l’eau (il a été démontré que certains œufs survivent à de longues périodes en contact avec de l’eau de mer), ou encore le transport d’œufs dans le tube digestif d’oiseaux insectivores. 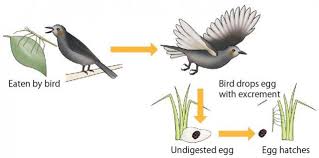 |
Bibliographie
- Simon S. et al. (2019) : Old world and new world Phasmatodea : phylogénomics resolve the evolutionary history of Stick and Leaf insects. Ecology and Evolution, V7 (lien)
- Chen S. et al. (2018) : The earliest Timematids in Burmese amber reveal diverse tarsal pads of stick insects in the mid-Cretaceous. Insect Science, 1-13 (lien)