Automédication parasitaire chez le Monarque
Par Fanny Vogelweith
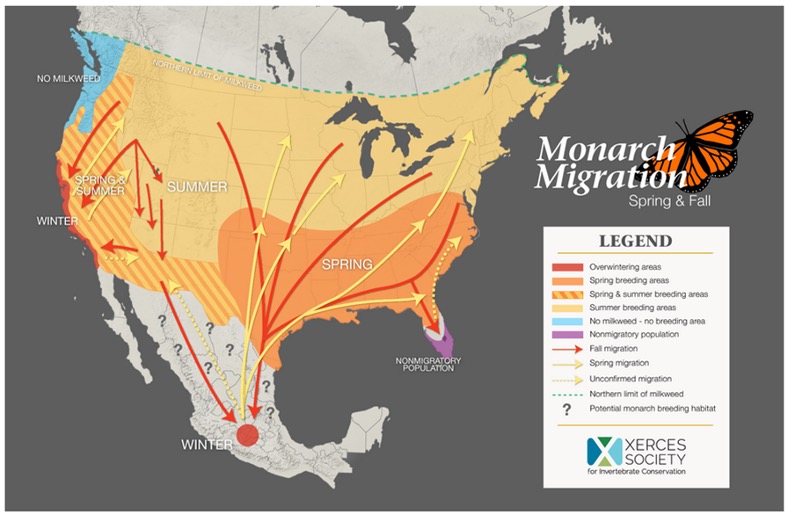
Le Monarque (Danaus plexippus), ce superbe papillon orange et noir (figure 1), pourrait à lui seul nous faire un cours d’écologie et d’évolution. Il est notamment connu pour sa grande migration annuelle où des millions d’individus quittent le Canada, en automne, pour rejoindre les forêts de la région mexicaine du Michoacan (figure 2). Le retour vers le nord se fera par plusieurs générations de descendants au printemps suivant.
Le Monarque (Danaus plexippus), ce superbe papillon orange et noir (figure 1), pourrait à lui seul nous faire un cours d’écologie et d’évolution. Il est notamment connu pour sa grande migration annuelle où des millions d’individus quittent le Canada, en automne, pour rejoindre les forêts de la région mexicaine du Michoacan (figure 2). Le retour vers le nord se fera par plusieurs générations de descendants au printemps suivant.
Cette migration qui requiert des capacités physiques impressionnantes, lui permet notamment de réduire de manière considérable les infections par des parasites, tel que le protozoaire spécialiste Ophryocystis elektroscirrha (OE) (figure 3).
Pourquoi ?
D’abord car la migration permet aux animaux d’échapper périodiquement aux parasites locaux, ensuite car elle favorise la sélection des individus résistants à ces parasites – les sujets infectés étant incapables de survivre à un tel périple. Hors migration, le Monarque reste tout de même exposé aux parasites.

Il a donc développé, parmi d’autres, une surprenante stratégie pour réduire les infections : l’automédication ou pharmacophagie (Encadré 1).
Encadré 1 L’automédication est la capacité à consommer ou à entrer en contact avec des composés organiques biologiquement actifs, dans le but d’aider à éliminer une infection parasitaire ou d’en réduire les symptômes. Pour être sûr qu’une espèce pratique l’automédication, il faut que les quatre critères suivants soient réunis : (1) Le composé doit être consommé de manière proactive ; (2) Il doit nuire à un ou plusieurs parasites ; (3) L’effet néfaste de ce composé sur les parasites doit avoir un effet positif sur l’hôte qui le consomme ; (4) Le composé doit avoir un effet néfaste sur son consommateur lorsqu’il est ingéré en absence de parasites.La consommation de ces composés peut se produire en prévention d’une infection, c’est l’automédication prophylactique. Par exemple, les fourmis rousses des bois (Formica rufa) incorporent une résine antimicrobienne provenant des conifères dans leurs nids, uniquement lorsque le risque de prolifération microbienne dans la colonie est élevé. L’automédication peut également être thérapeutique, lorsqu’elle est utilisée après une infection. Par exemple, les Orang-Outans (Pongo pygmaeus) s’appliquent des feuilles de Dracaena cantleyi mastiquées sur certaines blessures afin d’en réduire la douleur. |
Longtemps considérée comme anecdotique et anthropomorphique, l’automédication a ensuite été démontrée chez les grands singes tels que les Orang-Outans ou les Chimpanzés. L’automédication était donc censée être réservée aux animaux dotés de certaines capacités cognitives.
Cependant, depuis quelques années, les exemples se multiplient non seulement chez les vertébrés, à l’instar du mouton, mais également chez les insectes. Le monarque a été un des premiers modèles d’insectes où elle a été décrite, notamment grâce aux travaux de Jaap de Roode (Université d’Emory, Etats-Unis) et Thierry Lefèvre (IRD, France).
Désormais démontrée chez d’autres espèces d’insectes comme la drosophile (Drosophila melanogaster), la Noctuelle méditerranéenne (Spodoptera littoralis) ou encore chez l’abeille (Apis mellifera), l’automédication chez le Monarque reste un exemple phare.
De manière plus concrète, il a été montré que les femelles Monarque infectées par le protozoaire OE pondaient leurs œufs sur des feuilles d’asclépiades, réduisant ainsi l’infection parasitaire de leurs descendants (Figure 4).
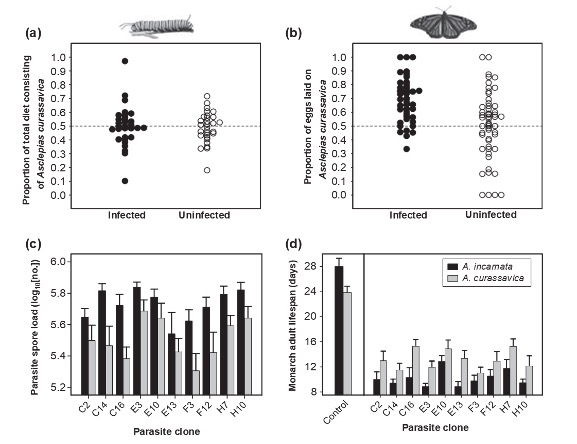
En effet, les chenilles (Figure 5) ne discriminent pas les plantes médicinales des autres, mais, elles se nourrissent de la plante où leur mère a pondu (Figure 5). Une fois leurs œufs éclos, les larves vont donc manger les feuilles d’asclépiades. Ces feuilles sont reconnues pour leur toxicité liées aux molécules alcaloïdes et cardénolides qu’elles renferment.
La production de ces molécules est un des mécanismes de défense de la plante suite à une attaque (ici, une attaque par un herbivore). Les cardénolides vont, notamment, causer la modification des acides aminés de la pompe sodium-potassium (Na+/K+ ATPase) présente sur de nombreuses cellules dont les cellules nerveuses. Ces modifications ont des conséquences souvent fatales pour les individus qui consomment les cardénolides.

Cependant, pour contrer cela, le Monarque a développé un panel de mécanismes de résistances allant de l’insensibilité au changement d’acides aminés dans la pompe sodium-potassium, en passant par la conversion des cardénolides en forme moins toxique grâce à la séquestration (encadré 2), et enfin par des mécanismes de détoxification (encadré 3) des composés toxiques impliquant de nombreuses protéines (cytochrome P450, glutathionne S-transférase, etc.).
Encadré 2 La notion de séquestration de composés de défenses des plantes par les insectes a été proposée dès 1893 par l’entomologiste allemand Erich Haase (1859 – 1894), précisément sur le modèle d’étude de cet article, le papillon Monarque.Depuis, cette hypothèse a été validée sur plus de 275 espèces d’insectes spécialistes. La séquestration est la capacité des herbivores à accumuler de manière sélective des composés toxiques de défenses des plantes afin de les détourner à leur avantage, pour leur propre défense. Ainsi les insectes ont développé des mécanismes qui leur permettent d’accumuler les composés des plantes dans différentes parties de leur corps tels que l’hémolymphe, des glandes exocrines, des compartiments sous-cuticulaire, leur tégument, etc. Par exemple, les larves de chrysomèles (Chrysomelina sp.) possèdent 9 paires de glandes de défenses exocrines sur leur dos reliées à un réservoir spécifique. En cas d’attaque, elles relâcheront des secrétions répulsives via ces glandes. Chez le Monarque, les cardénolides sont dégradés par le cytochrome P450 puis emmagasinés dans les intestins et le corps gras. Par l’intermédiaire de différents processus, le Monarque utilise les composés stockés dans son corps en se rendant immangeables pour ses prédateurs et en tuant ses parasites. |
Ainsi, là où d’autres insectes meurent intoxiqués, les chenilles de Monarque sont capables d’utiliser des composés toxiques pour leur propre défense contre leurs ennemis et ainsi combattre une infection parasitaire.
La femelle Monarque, de par son choix de ponte, va donc augmenter les chances de survie de sa descendance, c’est de l’automédication transgénérationnelle.
Cependant, malgré ses défenses sophistiquées, le Monarque est une espèce en déclin pour, notamment, trois raisons.
- La première est, de toute évidence, liée au changement climatique. Avec l’augmentation du C02 dans l’air, les espèces d’asclépiades les plus riches en cardénolides ont perdues leurs propriétés médicinales. En conséquence, la tolérance et la résistance des Monarques aux infections a diminué et la virulence du parasite a augmenté.
- La deuxième raison est également prévisible. L’association entre la déforestation et l’utilisation intensive d’herbicides à considérablement réduit la présence d’asclépiades. Sans nourriture suffisante, les populations de Monarque ne peuvent se maintenir.
- Enfin, la troisième raison résulte d’une initiative contre-productive. Face au déclin des Monarques et de leur plante hôte, de nombreux Américains ont décidé de planter des asclépiades. Cependant, l’espèce tropicale d’asclépiade commercialisée fleurie en hiver. Devant cette abondance de nourriture en hiver, les Monarques ne migrent plus et sont donc plus enclin à être parasités, favorisant leur déclin.
De ce fait, le Monarque est désormais classé parmi les espèces en danger, d’après l’IUCN. De nombreux plans de conservation de ce papillon ont été mis en place afin de le préserver.
Encadré 3 Le mécanisme de détoxification chez les insectes est un processus permettant de neutraliser et d’éliminer les substances toxiques, tels que les composés secondaires des plantes.Il se déroule en 3 phases :(1) la fonctionnalisation où les composés toxiques vont être modifiés par réactions enzymatiques successives (impliquant souvent les cytochromes P450) par oxydation, hydrolyse et réduction des molécules néfastes (2) la conjugaison où les composés modifiés sont liés à des molécules hydrophiles comme le glutathion, l’acide glucuronique ou des groupes sulfates, grâce à des enzymes comme les glutathion S-transférases ou les UDP-glucuronosyltransférases (3) l’excrétion où les substances toxiques transformées sont expulsées hors des cellules par des transporteurs spécifiques (comme les transporteurs ABC) et éliminées via le tube digestif, les tubules de Malpighi ou la cuticule. Dans de rares cas, ces substances peuvent être réutilisées. Par exemple, certaines espèces de Scolytes détoxifient les monoterpènes des résines de leurs hôtes en les hydroxylant en alcools, puis en les libérant sous forme de phéromones d’agrégation afin de recruter des congénères dans un environnement favorable. |
Bibliographie
- Abbott, J. (2014) : Self‐medication in insects: current evidence and future perspectives. Ecological Entomology, 39(3), 273-280 (lien)
- Agrawal, A.A., Petschenka, G., Bingham, R.A., Weber, M. G. & Rasmann, S. (2012) : Toxic cardenolides: chemical ecology and coevolution of specialized plant–herbivore interactions. New Phytologist, 194, 28–45 (lien)
- Bartel, R.A., Oberhauser, K.S., de Roode, J.C. & Altizer, S.M. (2011) : Monarch butterfly migration and parasite transmission in eastern North America. Ecology, 92(2), 342-351 (lien)
- Beran, F. & Petschenka, G. (2022) : Sequestration of Plant Defense Compounds by Insects: From Mechanisms to Insect–Plant Coevolution. Annual Review of Entomology, 67, 163-182 (lien)
- Castella, G., Chapuisat, M. & Christe, P. (2008) : Prophylaxis with resin in wood ants. Animal Behaviour, 75, 1591-1596 (lien)
- De Roode, J.C., Lefèvre, T., & Hunter, M. D. (2013) : Self-medication in animals. Science, 340(6129), 150-151 (lien)
- Erler, S., Cotter, S. C., Freitak, D., Koch, H., Palmer-Young, E. C., de Roode, J. C., … & Lattorff, H. M. G. (2024) : Insects’ essential role in understanding and broadening animal medication. Trends in Parasitology, 40(4), 338-349 (lien)
- Lefèvre, T., Oliver, L., Hunter, M.D. & de Roode, J.C. (2010) : Evidence for trans-generational medication in nature. Ecology Letters, 13, 1485-1493 (lien)
- Morrogh-Bernard, H.C., Foitová, I., Yeen, Z., Wilkin, P., de Martin, R., Rárová, L., Doležal, K., Nurcahyo, W. & Olšansky, M. (2017) : Self-medication by orang-utans (Pongo pygmaeus) using bioactive properties of Dracaena cantleyi. Scientific Report,7:16653 (lien)
- Petschenka, G., Fandrich, S., Sander, N., Wagschal, V., Boppré, M., & Dobler, S. (2013) : Stepwise evolution of resistance to toxic cardenolides via genetic substitutions in the Na+/K+-ATPase of milkweed butterflies (Lepidoptera: Danaini). Evolution, 67(9), 2753–2761 (lien)
- Tan, W.-H., Acevedo, T., Harris, E. V., Alcaide, T. Y., Walters, J. R., Hunter, M. D., Gerardo, N. M., & de Roode, J. C. (2019) : Transcriptomics of monarch butterflies (Danaus plexippus) reveals that toxic host plants alter expression of detoxification genes and down-regulate a small number of immune genes. Molecular Ecology, 28(22), 4845–4863 (lien)